
(4)A、B、C、D四个试剂瓶中别离盛碳酸钠、硝酸银、烧碱、稀硫酸四种稀溶液中的一种,取四种溶液各少数,顺次滴入物质X的溶液和稀硝酸,发生的现象如表所示:
②物质B是,参加X后反响的化学方程式是,加稀硝酸后,沉积消失的反响化学方程式是.
(2)大理石为碳酸钙、纯碱为碳酸钠的俗称、烧碱为氢氧化钠、铜绿为碱式碳酸铜、胆矾为五水硫酸铜,据此写出化学式;
(4)①依据不溶于硝酸的沉积有:氯化银和硫酸钡,参加的X纪要供给氯离子,也要供给钡离子,所以X便是氯化钡,A和C是硫酸和硝酸银;
②依据X是氯化钡,B和氯化钡会生成沉积,沉积又会溶于硝酸生成气体,所以B便是碳酸钠,D便是氢氧化钠,依据推出的反响物、生成物书写化学方程式;
③依据硫酸和硝酸银不同的性质进行规划.回答:解:(1)依据在化合物中正负化合价代数和为零,可得:
(3)硝酸为化学式为HNO3、碳酸氢钙的化学式为Ca(HCO3)2、高锰酸钾的化学式为KMnO4、硫酸钡的化学式为BaSO4、硫酸铝的化学式为Al2(SO4)3,
(4)①学过的不溶于硝酸的沉积有:氯化银和硫酸钡,参加的X既要供给氯离子,也要供给钡离子,所以X便是氯化钡,A和C是硫酸和硝酸银,
②X是氯化钡,B和氯化钡会生成沉积,沉积又会溶于硝酸生成气体,所以B便是碳酸钠,参加X后反响的化学方程式是:Na2CO3+BaCl2=BaCO3↓+2NaCl;加稀硝酸后,沉积消失的反响化学方程式是:BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑,
③生动的金属会与酸反响生成氢气,而硝酸银不会,反响的化学方程式为:Fe+2AgNO3=Fe(NO3)2+2Ag
(3)将amolQ单质与bmolR单质组成的固体混合物投入到足量的水中,若固体彻底溶解终究得到弄清溶液,则一起发生的气体的物质的量为mol(用a、b表明);当a=b时,写出反响的离子方程式.
(4)①和⑨的最高价氧化物对应水化物的化学式为和.①和⑨两元素构成化合物的化学式为;该化合物灼烧时的焰色为色;该化合物的溶液与元素⑧的单质反响的化学方程式为.
(5)①和⑤最高价氧化物对应水化物彼此反响的化学方程式为;离子方程式为.
(6)用电子式表明第三周期元素中由电负性最小的元素和电负性最大的元素构成化合物的进程.
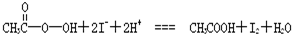
(l)配应①的离子方程式(配平系数填入以下方框内):□MnO4-+□H2O2+□H+═□Mn2++□O2十□H2O
(3)取b0mL待测液,用硫酸使溶液酸化,再用浓度为a1mol?L-1的KMnO4标准溶液滴定其间的H2O2,耗用的KMnO4体积为b1mL(反响①,滴定进程中KMnO4不与过氧乙酸反响);
另取b0mL待测液,参加过量的KI,并用硫酸使溶液酸化,此刻过氧乙酸和残留的H2O2都能跟KI反响生成I2(反响②和③);
请依据上述试验数据核算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表明).c0=.
(4)为核算待测液中过氧乙酸的浓度c0,参加的KI的质量已过量但没精确称量,影不影响测定成果(填是或否)